Mitten im Herzen der Metropole konzentriert sich die KÖ-Aesthetics Schönheitschirurgie in Düsseldorf seit 2007 auf unterschiedliche Behandlungen im Bereich der Plastischen und Ästhetischen Chirurgie.
Durchschnittliche Jameda-Bewertung


Die Zufriedenheit unserer zahlreichen Patientinnen und Patienten unterstreicht die Kompetenz unserer Fachärzte, die sich in unserer Praxisklinik auf sehr vielfältige Behandlungen und Eingriffe aus der Plastischen und Ästhetischen Chirurgie konzentrieren. Im Mittelpunkt unserer Arbeit steht jederzeit Ihre Gesundheit und Ihr Wohlbefinden. Zugleich haben Ihre Individualität und Wünsche höchste Priorität für uns, damit wir stets ein optimales Ergebnis für Sie erzielen!
Neben der Plastischen & Ästhetischen Chirurgie führen wir bei KÖ-Aesthetics auch viele medizinisch notwendigen Eingriffe im Rahmen der Rekonstruktiven Chirurgie durch. Im Laufe des Werdegangs unseres Chefarztes Herrn Hosseini, arbeitete er auch im Bereich der Handchirurgie oder auch Verbrennungschirurgie, zu Behandlung nach Unfällen oder auch von Narben. Auf diese umfangreiche Expertise vertrauen unsere Patientinnen und Patienten seit über 15 Jahren.
Sensibel und offen für Ihre Wünsche.

Unsere kompetenten Mitarbeiter und Ärzte sorgen jederzeit mit vollem Einsatz für Ihre Sicherheit und ein optimales Ergebnis. In unserer Praxisklinik für Plastische Chirurgie in Düsseldorf erwartet Sie ein erfahrenes Team von Fachärzten in einem freundlichen Ambiente.
Die klassische Plastische Chirurgie beschäftigt sich mit der chirurgischen Verbesserung des Erscheinungsbildes aus funktionellen oder ästhetischen Gründen. Durch die ständige Neu- und Weiterentwicklung moderner Methoden, Geräte und Hilfsmittel kommen heutzutage immer mehr Behandlungen auch ohne einen operativen Eingriff und damit ohne Schnitte und Narkose aus.
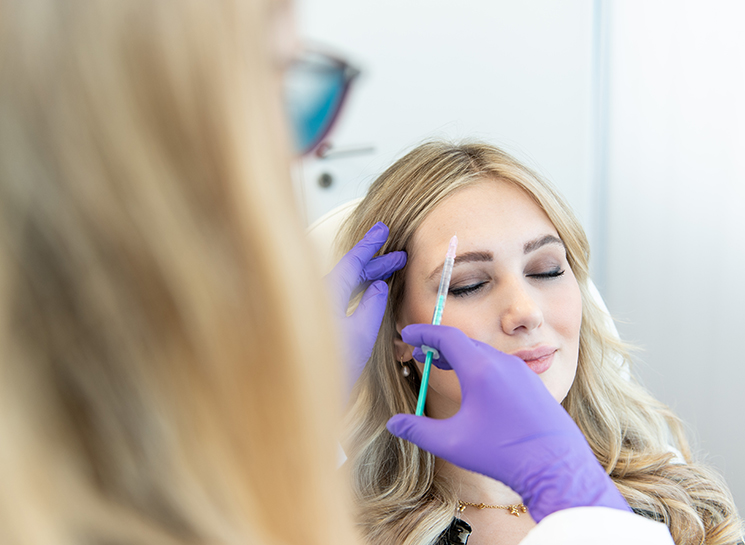


Schönheitschirurgie bildet im medizinischen Fachbereich mittlerweile eine immer wichtigere Bedeutung. Der Wunsch, kleine Makel des eigenen Körpers zu optimieren und anzupassen, ist nicht weiter ungewöhnlich und ebenso nicht verwerflich. Dabei bietet die Ästhetisch-Plastische Chirurgie sowohl für Frauen als auch für Männer die Option, Eingriffe vorzunehmen. Hohe Priorität in der Schönheitschirurgie und Praxisklinik in Düsseldorf genießt dabei die persönliche Beratung und Unterstützung. Sowohl vor der Behandlung als auch danach. Vertrauen in die Leistung unserer Fachärzte ist für uns daher besonders wichtig. Wir möchten Ihre Erwartungen, die Sie hinsichtlich des chirurgischen Eingriffs hegen, erfüllen können. Dabei bietet das KÖ-Aesthetics Fachzentrum für Schönheitschirurgie ein denkbar breit gefächertes Spektrum an unterschiedlichen Eingriffen.
Das schließt allerdings viele weitere Eingriffe, die zur Korrektur kleinerer und größerer Schönheitsmakel dienen, nicht automatisch aus. So werden in der Praxisklinik auch Nasenkorrekturen sowie Profilkorrekturen und Ohranlegungen durchgeführt. Auch Haartransplantationen sowie Bauchdeckenstraffungen werden von unseren Fachärzten umgesetzt. Welche Eingriffe hier am häufigsten gefragt sind, unterscheidet sich von Patient zu Patient recht stark. Natürlich können Sie auch mehrere chirurgische Behandlungen ins Auge fassen. Gerne beraten Sie unsere Ärzte in der Praxisklinik und zeigen Ihnen auf, welche Möglichkeiten Ihnen offen stehen.

In der Schönheitschirurgie Düsseldorf helfen uns Erfahrungswerte aber auch moderne und ausgereifte Technik, Kosmetische Eingriffe zu realisieren, die zur im vollen Umfang zur Patientenzufriedenheit beitragen sollen.
Im Vorfeld einer Schönheits OP ist ein persönliches Gespräch mit dem behandelnden Arzt unentbehrlich. In der Praxisklinik in Düsseldorf legt unser Ärzte Team daher besonders großen Wert darauf, individuell bereits im Vorfeld auf den Patienten einzugehen und dabei über Wünsche, Erwartungen aber auch mögliche Risiken zu sprechen.
Ihre Zufriedenheit als Patient genießt höchste Priorität. Vertrauen schaffen wir dabei durch unsere modern ausgestattete Schönheitsklinik sowie durch transparenten Leistungen und Preise, die unsere uneingeschränkt qualifizierten medizinischen Leistungen unserer Schönheits-OPs in Düsseldorf zusätzlich untermauern.
Unsere moderne Praxis liegt mitten im Herzen von Düsseldorf mit bequemen Parkmöglichkeiten in der Tiefgarage.


„Viele unserer Patienten empfehlen uns weiter. Und einige nehmen selbst lange Fahrzeiten gerne in Kauf, weil sie sich in unserer Praxisklinik sehr gut betreut und behandelt fühlen!“, so Massud Hosseini, der KÖ-AESTHETICS vor über 15 Jahren gegründet hat.
Der Facharzt für Plastische und Ästhetische Chirurgie wurde im Iran geboren und kam als Kind mit seinen Eltern nach Deutschland. Sein Studium der Humanmedizin führte ihn nach Aachen, Göttingen, Bonn und nach Houston, Texas. Auch sein praktisches Jahr verbrachte er teils in Deutschland, teils in den USA.
Seit nun über 15 Jahren beweist die Schönheitschirurgie KÖ-Aesthetics in Düsseldorf ihre Expertise im Hinblick auf Eingriffe im Bereich der Ästhetisch-Plastischen Chirurgie. Schönheitschirurgie auf höchstem Facharzt-Niveau schaffte in der Vergangenheit bis heute das nötige Vertrauen, weshalb das Team von KÖ-Aesthetics stolz sein kann auf zahlreiche zufriedene Patienten. Vorteilhaft ist zusätzlich die zentrale Lage der modern ausgestatteten Schönheitsklinik in Düsseldorf, welche sich direkt zentral in der Metropole befindet. Wichtige Faktoren für unseren Erfolg sind das erfahrene Praxis-Team inklusive renommierter Fachärzte, die sich auf unterschiedliche Behandlungen spezialisiert haben. So findet sich für nahezu jeden gewünschten chirurgischen Eingriff auch der richtige Experte. Gerne begrüßen wir Sie in unseren Klinikräumen, in denen wir durch eine stimmige Einrichtung und persönliche Beratung für eine besonders entspannte und angenehme Atmosphäre sorgen möchten.



Auch die Schönheitschirurgie befindet sich in einem stetigen Wandel. Behandlungsmethoden und Eingriffe sind in den vergangen Jahrzehnten recht deutlich verbessert worden. Die Zielsetzung sind möglichst kleine Eingriffe mit einem maximalen Effekt, wobei die Sicherheit des Patienten oberste Priorität genießt. In der Schönheitschirurgie Düsseldorf helfen uns Erfahrungswerte aber auch moderne und ausgereifte Technik, Kosmetische Eingriffe zu realisieren, die zur im vollen Umfang zur Patientenzufriedenheit beitragen sollen.
Wir arbeiten ständig daran, die Ausstattung der Praxisklinik zu optimieren und um die neusten und wichtigsten Medizingeräte zu ergänzen. Unentbehrlich, um für eine sichere und qualifizierte medizinische Behandlung und Betreuung zu sorgen. Auch unser Team und unsere Ärzte sind ständig bestrebt, ihr Wissen rund um die Ästhetisch-Plastische Chirurgie auch lange nach dem Studium und der Ausbildung auszubauen.
Schönheitschirurgie verbinden viele automatisch mit hohen Kosten. Somit stellt sich auch in Ihrem Fall womöglich die Frage, ob Sie sich einen solchen Eingriff überhaupt leisten können. Der Wunsch nach einem schöneren Körper muss aber kein Luxusgut sein. Die Zeit, in der Schönheitschirurgie ausschließlich Patienten mit einem flexiblen Budget vorbehalten war, ist lange vorbei. Auch in in der Schönheitschirurgie Düsseldorf verfolgen wir diese Zielsetzung und möchten Eingriffe in unserem Fachzentrum deutlich einfacher zugänglich machen. Von erschwinglichen Preisen zu profitieren, heißt in dem Fall aber nicht automatisch, dass qualitative Abstriche einzuplanen sind. Sie erhalten in der Praxisklinik ein umfassendes medizinisches Leistungspaket und ganzheitliche Betreuung durch unsere qualifiziert ausgebildeten Ärzte.

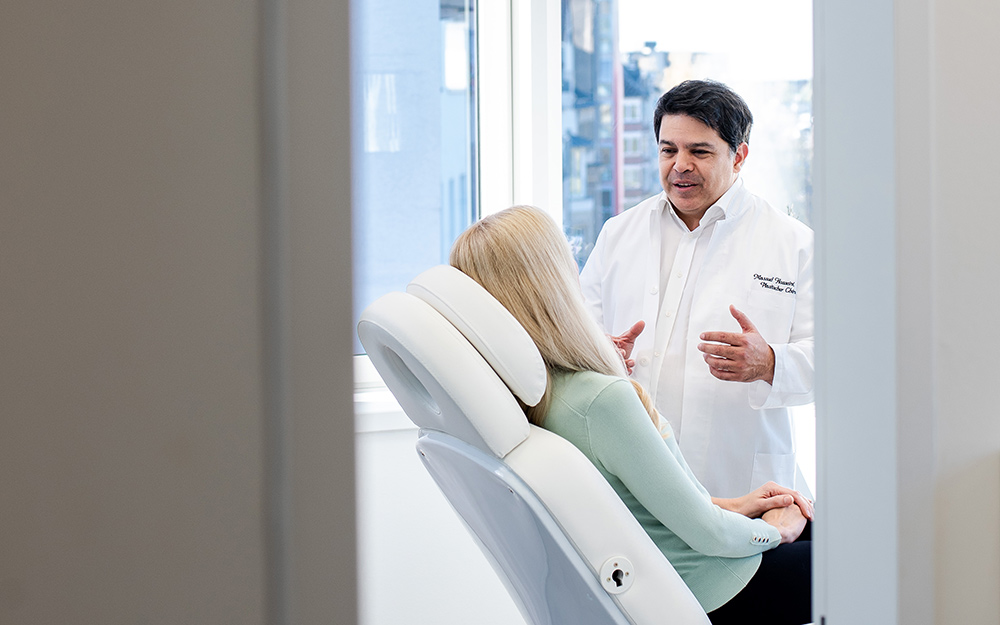

Im Vorfeld einer Schönheits OP ist ein persönliches Gespräch mit dem behandelnden Arzt unentbehrlich. In der Praxisklinik in Düsseldorf legt unser Ärzte Team daher besonders großen Wert darauf, individuell bereits im Vorfeld auf den Patienten einzugehen und dabei über Wünsche, Erwartungen aber auch mögliche Risiken zu sprechen. Natürlich ist eine Kosmetische Operation mit vielen Vorteilen verbunden, es gilt aber auch Risiken abzuwägen und zu klären, ob die Erwartungen des Patienten vielleicht zu groß sind. Eine Schönheitsoperation wird nach dem Eingriff oft nur subjektiv wahrgenommen. Daher ist der Wunsch nach einer solchen Operation häufig darauf zurückzuführen, dass sich der Patient an eigenen kleinen Fehlern des Körpers stört, die anderen womöglich gar nicht auffallen. Dennoch ist der Wunsch nach einer solchen Operation nicht unberechtigt und kann individuell mit dem medizinischen Spezialisten für den jeweiligen Eingriff, direkt besprochen werden. Natürlich ist das Gespräch absolut vertraulich und unser Team versucht, Ihre Fragen und Unklarheiten nach bestem Gewissen zu beantworten.
Schönheitschirurgie verbinden viele automatisch mit hohen Kosten. Noch immer gilt die Ästhetisch-Plastische Chirurgie und die damit verbundenen Behandlungsmethoden als medizinisches Luxusgut. Dabei dient die moderne Schönheitschirurgie nicht nur dem Zweck, den Körper zu verschönern. Auch in Hinblick auf psychologische Aspekte, nehmen Schönheitsoperationen und Korrekturen einen immer wichtigeren Stellenwert ein. Das Ziel ist es, dem Patienten neues Selbstvertrauen zu verleihen und dazu beizutragen, dass sich dieser wieder wohl in seiner eigenen Haut fühlt. Oft kann das allein von einer Nasenkorrektur oder Fettabsaugung abhängen und die Lebensqualität des Betroffen deutlich steigern. Das gelingt beispielsweise, durch Fettabsaugungen nach einer erfolgreichen Diät oder auch durch ästhetische Eingriffe nach einem Unfall.
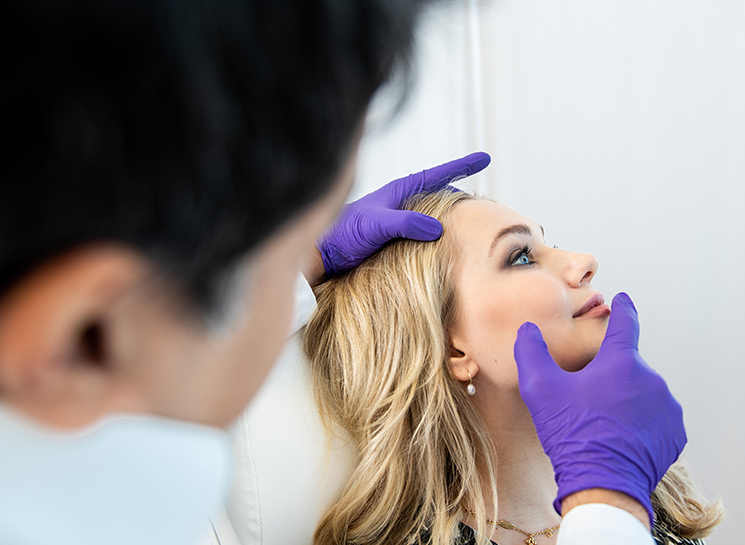






Ein großer Vorteil der Praxisklinik KÖ-Aesthetics in Düsseldorf ist die zentrale Lage direkt im Herzen der belebten Metropole Düsseldorf. Vor allem wenn Sie von außerhalb anreisen, ist die Anfahrt für Sie daher denkbar unkompliziert. Vom Bahnhof und Flughafen aus, können Sie die Klinik schnell und unkompliziert erreichen. Wer mit dem eigenen PKW anreist, kann hingegen einfach in der Tiefgarage des Gebäudes parken.
Die KÖ-Aesthetics Schönheitschirurgie in Düsseldorf bietet in zentraler Lage direkt in der belebten Metropole umfassende Leistungen rund um die Ästhetisch-Plastische Chirurgie an. Als Fachzentrum für Ästhetische-Plastische Chirurgie konnte die Praxis in den vergangenen 15 Jahren bereits über 38.000 Patienten/-innen überzeugen. Auch Ihr Vertrauen in unsere Leistung und kompetente Beratung liegt uns am Herzen. Gerne bieten wir Ihnen eine erste und unverbindliche Beratung, wenn Sie Fragen zu den individuellen Behandlungen und Optionen in unserer Praxis haben. Am unkompliziertesten gestaltet sich die erste Kontaktaufnahme telefonisch. Sie erreichen uns von Montag bis Freitag immer in der Zeit zwischen 07:00 – 19:00 Uhr. Wahlweise kann ein Termin für ein erstes persönliches Beratungsgespräch auch online gebucht werden. Gerne nehmen wir Ihre Anfrage entgegen und klären alle weiteren Details und Unklarheiten in Hinblick auf Behandlungsoptionen in unserer Praxis.

Bei KÖ-AESTHETICS legen wir großen Wert auf Qualität – sowohl bei unseren Behandlungen als auch bei der Patientenberatung. Dies spiegelt sich auch in einem hohen Zufriedenheitsgrad unserer Besucher und Patienten wieder.
Werfen Sie einen Blick auf die zahlreichen positiven Feedbacks bei jameda und buchen Sie direkt online einen Termin!
Unser Fachärzte-Team kümmert sich um Ihr Anliegen
und berät Sie jederzeit umfassend und individuell!
Mit diesem Formular können Sie uns Fotos zusenden. Wir machen Ihnen gern einen unverbindlichen Vorschlag zu möglichen Behandlungen.
Folgen Sie uns auf unserem Instagram-Kanal und verpassen Sie keine Neuigkeiten mehr. Wir veröffentlichen regelmäßig Postings zu Behandlungen mit und ohne OP.